编者按:在本次ASH年会上与2020年5-8日在线上举行。在这项血液学“盛宴”汇聚了全球各地的血液肿瘤专家和学者,多项重磅级的研究公布了临床数据。既往骨髓瘤治疗已取得许多进展,但诸多关于BCMA CAR-T在骨髓瘤中的研究公布结果,亮点颇多。《肿瘤瞭望》特邀上海长征医院侯健教授进行点评、姜金星医生翻译这两项摘要。
一、#130.Spectrum of Hematological Malignancies in 130 Patients with Germline Predisposition Syndromes - Mayo Clinic Germline Predisposition Study
130 复发难治性多发性骨髓瘤病人的抗BCMA CAR-T细胞治疗bb21217 I期CRB-402研究的结果更新:治疗缓解持续时间和强度与T细胞表型的相关性
本研究旨在评价产品的特性跟包括持续缓解时间(DOR)的临床结局是否相关的一项对患者DPs分子特性的研究。
CRB-402 (NCT03274219)是一项正在进行的、多中心的、剂量递增的1期临床研究,针对的是复发难治性多发性骨髓瘤(RRMM)病人。受试者需满足:既往接受过至少3次包括蛋白酶体抑制剂和免疫调节剂的治疗,或者对蛋白酶体抑制剂和免疫调节剂双重耐药。在扩展队列(expansion cohort)中,受试者还需满足既往接受抗CD38抗体治疗并且对最后一次治疗方案耐药。
按计划入组74个病人,其中50人在扩展队列。病人先进行氟达拉滨(30 mg/m2) 和环磷酰胺(300 mg/m2)淋巴细胞耗竭的预处理,然后接受150×106,300×106或450×106剂量的CAR-T bb21217的输注。临床结局的主要观察指标是不良事件(AEs)的发生率,包括剂量限制性毒性(DLTs)。其他临床结局的指标包括按国际骨髓瘤工作组统一反应标准规定的总体反应率和持续缓解时间。我们通过RNAseq和cyTOF描述DP和血液单采外周血单个核细胞(PBMC),并且将从单采血液到药物产品中记忆/衰老标志的表达与包括缓解持续时间在内的临床结局相关联。
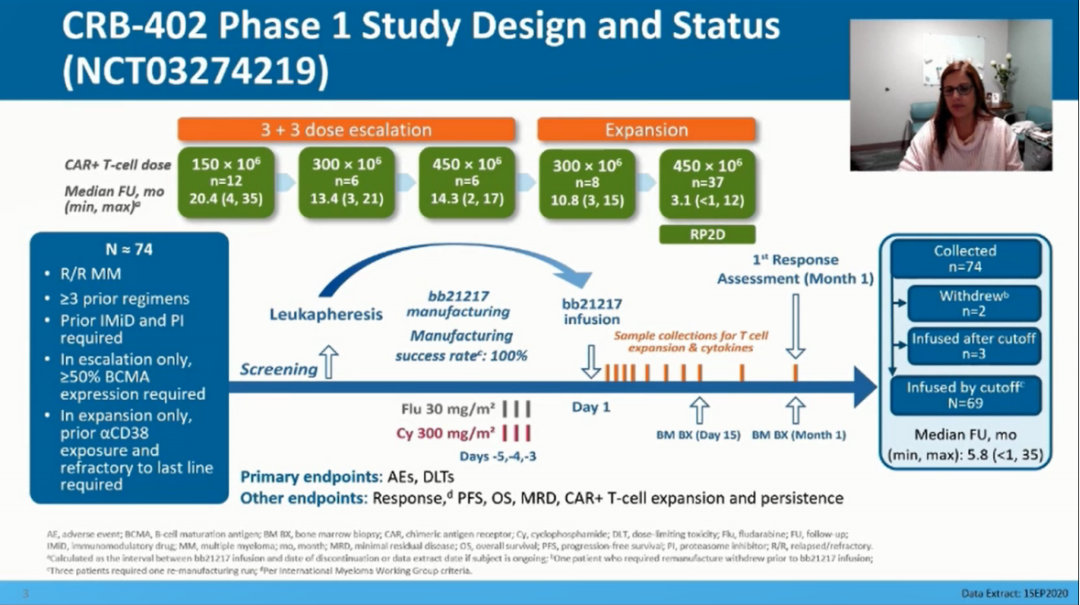
截止2020年3月1日入组46例病人(中位年龄62[范围:33-74])接受bb21217治疗,其中24例在剂量递增(12例-150×106,6例-300×106,6例-450×106),22例在扩展队列(8例-300×106,14例-450×106),所有病人的中位随访时间为8.5(<1-29)月。病人的中位既往治疗线数为6(3-17)并且26/46(57%)的病人表现为三重耐药。
安全性方面:①31/46(67%)的病人发生细胞因子释放综合征(CRS),包括1例死亡病例(14例1级,15例2级,1例3级以及1例5级),距离第一次发作的中位时间是3(1-20)天,并且应用托珠单抗(18例)+/-糖皮质激素(6例)治疗CRS。
②10例病人(22%)发生神经毒性(5例1级,2例2级,2例3级,1例4级),第一次发作距离CAR-T细胞治疗的中位时间为7(3-14)天。
有效性方面:①研究者对44个病人至少随访2个月后评估治疗反应,或者病人出现两个月内病情进展/死亡。根据国际骨髓瘤工作组标准确定24例(55%)病人的治疗反应,包括8例(18%)≥CR和13例VGPR。出现CR的中位时间为2.5(1-24)月。
②在接受目标剂量在150-450*106的CAR-T细胞治疗的病人中,中位DOR为11.9(95% CI: 8.1-17.0)。目标剂量为450*106的CAR-T细胞被选为II其临床研究确定剂量并且正在进行剂量扩增。
③对44例病人的bb21217 药物产品进行了特征分析,PBMC和药物产品中T细胞的成对分析提示在bb21217 药物产品中记忆样T细胞(LEF1+, CD27+, CCR7+)明显增多,而高分化或衰老T细胞(CD57+)减少。当病人输注的药物产品中T细胞高表达早期记忆标志(LEF1+, CCR7+ and CD27+)以及低表达效应/耗竭标志(EOMES+, GZMA+, CD57+),病人出现CAR-T细胞扩增高峰的可能性较大。为了研究这些药物产品标志与DOR之间的关系,我们通过中位标志的表达(高或低)将24例治疗后反应≥PR的病人分开,并且分析在这些不同亚群中DOR的情况。CD127的高表达与持续T记忆细胞的生成有关,并且跟DOR呈正相关,而很多与T细胞分化相关的标记(如EOMES+,TBET+)与DOR负相关。
该研究中观察到的不良事件与已知CAR-T细胞治疗后的细胞毒性副反应一致。最初bb21217的治疗有效性是令人振奋的,接受150×106-450×106目标剂量治疗的病人中48%出现≥VGPR。并且研究发现药物产品中呈现和T细胞记忆相关的标志且缺失和T细胞分化/衰老相关的标志与T细胞在体内的扩增高峰和DOR呈正相关。
多发性骨髓瘤(MM)目前仍然不能治愈,其原因之一是患者免疫功能受抑,不能发挥免疫监督功能,导致MM反反复复而不治。抗BCMA CAR-T细胞治疗在复发难治性多发性骨髓瘤(RRMM)患者的治疗中具有巨大的潜力。Bb21217是一种抗BCMA CAR-T细胞治疗,它应用idecabtagene vicleucel (bb2121)一样的CAR分子,但是在体外扩增记忆性样T细胞的药物产品时加入PI3K抑制剂bb007,因此减少了高分化或者衰老T细胞的比例。研究发现MM特异的T淋巴细胞克隆处于衰老状态而出现低反应。过继性细胞免疫治疗可激活和扩增MM 特异的T淋巴细胞以提供持久的肿瘤免疫监视,是有希望改善治疗效果MM的治疗策略。CRB-402研究通过在CAR-T成品药物中增加记忆样T细胞的比例,降低衰老T细胞的比例,拟期待增强CAR-T的疗效。本临床研究结果表明接受bb21217治疗的病人48%s≥VGPR,且bb21217中记忆样T细胞的比例与DOR呈正相关,证明减少衰老T细胞的比例的确可以达到增强CAR-T疗效的作用,这为CAR-T治愈RRMM患者提供了新的思路。
二、131.Idecabtagene Vicleucel (ide-cel, bb2121), a BCMA-Directed CAR T Cell Therapy, in Patients with Relapsed and Refractory Multiple Myeloma: Updated Results from Phase 1 CRB-401 Study
复发难治性多发性骨髓瘤病人的抗BCMA CAR-T细胞治疗—Idecabtagene Vicleucel (ide-cel, bb2121):I期CRB-401临床研究的数据更新
ide-cel是一种抗BCMA CAR-T细胞治疗,在第一次应用在人类中的I期CRB-401临床研究(Raje et al. N Engl J Med. 2019; 380: 1726) 和关键的II期KarMMa临床研究 (Munshi et al. J Clin Oncol. 2020;38[suppl, abstr]:8503)中治疗复发难治性多发性骨髓瘤(RRMM)病人,显示出其良好的耐受性和巨大的治疗潜力。ide-cel展现出良好的风险-收益比,表现为总反应率(ORR)达85%,完全缓解率达45%,以及在CRB-401临床研究中第一批33例治疗病人的中位无进展生存期为11.8月。这里我们将汇报正在进行的CRB-401临床研究中接受ide-cel治疗的62例病人的有效性和安全性的更新数据。
CRB-401(NCT02658929)是一项包括剂量递增和扩展的I期临床研究。扩展阶段入组病人需满足以下条件:既往接受过至少三线包括蛋白酶体抑制剂、免疫调节剂和抗CD38抗体在内的治疗,且对最后一线耐药。剂量递增阶段的合格标准详见(Raje et al. N Engl J Med. 2019; 380: 1726)。病人先进行氟达拉滨(30 mg/m2)和环磷酰胺(300 mg/m2)×3天淋巴细胞剔除的预处理,在休息2天后接受剂量递增阶段目标剂量在50 ×106 , 150 × 106 , 450 ×106 , 或 800 ×106 CAR-T细胞的ide-cel治疗以及剂量扩展阶段150-450× 106剂量 CAR- T细胞的ide-cel治疗。研究主要终点是安全性,根据国际骨髓瘤工作组标准,次要终点包括治疗反应,探索性终点包括无进展生存期(PFS)、总生存率(OS)和最小残留疾病(MRD)。

截止2020年1月14日,剂量递增阶段招募21例病人,剂量扩展阶段招募41例病人,中位年龄为61岁,并且44%的病人肿瘤负荷高(骨髓中CD138+浆细胞≥50%)。在这62例病人中,45%既往接受过至少6次治疗方案,90%接受CD38单抗治疗且77%的病人对CD38单抗耐药。截止观察时,13例病人还在继续治疗和观察中,而49例已经退出结束了该次研究。结束研究的原因包括:病情进展(58%),病人自行退组(10%)以及死亡(10%)。根据剂量递增阶段的安全性和有效性,我们选择剂量扩展阶段的目标剂量为150-450×106 CAR+ T细胞。
在安全性方面:不良事件是中性粒细胞减少(92%),细胞因子释放综合征(CRS;76%),贫血(76%)以及血小板减少(74%)。最常见的3/4级不良事件是中性粒细胞减少(89%),白细胞减少(61%),贫血(57%)和血小板减少(57%)。大多数CRS不良事件是1级或2级。4个病人出现3级CRS,没有大于3级的CRS不良事件。CRS的发生率一般与目标剂量呈正相关。27例病人(44%)出现神经毒性,其中主要是1/2级不良事件,1例3级,1例4级。
有效性方面:在剂量递增和剂量扩展阶段的62名病人中总反应率为76%,包括24例(39%)CR或更好,40例(65%)VGPR或更好。中位缓解持续时间(DOR)为10.3月。在37例有反应的病人中进行最小残留疾病(MRD)检测,其中30例在1个或更多的时间点MRD阴性(≤10-4 有核细胞),其他7例均为MRD阳性。在剂量递增和剂量扩展阶段的所有病人中位随访时间为14.7月中,中位PFS为8.8月,中位OS为34.2月。综上所述,我们观察治疗反应和生存结局与剂量呈正相关,并且在≥150 ×106CAR+ T细胞剂量时疗效更好。

在多次既往治疗的RRMM患者中,Ide-cel治疗表现出良好且持久的治疗反应。疗效和安全性跟先前报告一致,并提出在目标剂量水平≥150×106 CAR+T细胞时ide-cel具有良好的临床效益-风险预测。
CAR-T治疗多发性骨髓瘤是近年来最引人瞩目的进展之一,目前中国、美国多个研究中心都在做关于CAR-T治疗复发难治性多发性骨髓瘤的研究。而这次更新数据为其在临床的应用奠定了坚实的基础。研究中多纳入了多线治疗失败的患者,从有效性上来看整体治疗效果较为显著且呈现与剂量一定相关性,且在高剂量组中耐受性尚可,这位以后研究中确定最佳治疗剂量提供了重要的依据。
上海交通大学医学院附属仁济医院血液科
国际骨髓瘤工作组(IMWG)委员
中华医学会血液学分会常委
中国抗癌协会血液肿瘤专委会常委
中国医师协会血液科分会常委、中国医师协会肿瘤科分会委员
CSCO中国抗淋巴瘤联盟常委、CSCO中国抗白血病联盟副主委
中国病理生理学会实验血液学分会委员
中国免疫学会血液免疫分会常委
上海医学会第10届血液学分会主委
上海免疫学会血液免疫专委会主委
中国医药创新促进会药物临床研究专委会副主委





 京公网安备 11010502033352号
京公网安备 11010502033352号